什么是完美气体?
完美的气体或理想气体是一种物质的状态,其液态的蒸发完成,并且严格在所有压力和温度条件下遵守所有气体定律。实际上,在所有压力和温度条件下,没有理想或完美的气体遵守所有气体定律。但是真正的气体,如氧气,氢气,氮气和空气,普通难以液化;在某些压力范围内和温度范围内可被认为是完美的气体(或理想的气体)
气体的物理性质由三个变量控制,它们是
- 气体施加的压力,
- 气体占据的容量
- 气体温度。
理想气体的行为可以用以下气体定律来研究,这些定律是由实验结果证明的。
- 波义耳氏定律
- 查尔斯的法律
- 吕萨克定律
让我们详细讨论一下气体的这些定律
博伊尔的法律
这项法律是由罗伯特·博伊尔在1662年制定的。
陈述:
它说明在恒定温度下,一个给定质量的理想气体的绝对压强与它的体积成反比。
在数学上

后缀1、2和3…表示不同的条件集。
解释:
为了理解这条定律,我们做个实验吧。

假设我们有一个圆筒活塞组件,其包含气体。如果我们通过施加外力比汽缸内部的气体的压力施加外力,请将该系统保持在室温(使温度保持恒定)。如果除去外部载荷,则大于气体的体积,则开始增加和压力将降低。这证明了,当完美气体的压力比其体积增加时,减少并且当体积降低时,压力增加。
查尔斯的法律
这项法律是由法国人雅克·a·c·查尔斯于1787年颁布的。
声明
本法可以用两种方式说明
声明1
在恒定的绝对压力下,完美气体的给定质量的体积直接变化到其温度。
解释:

让我们再拿一个保存在室温下的活塞汽缸总成。活塞的上部暴露在大气压力下(因此系统保持恒定的绝对压力)。圆筒的下部是热的导体。现在加热圆筒底部。一段时间后,气缸的活塞开始向上运动。为什么会发生这种情况?你能猜到吗?让我告诉你到底发生了什么。当气缸受热时,气缸内的气体温度升高,压力也增大,使得气体膨胀,对活塞施加一个力,使活塞向上运动。活塞向上运动以保持压力恒定(即气体内部压力与大气压力相等)。 The upward movement of the piston increases the volume of the gas
因此,我们可以得出结论,当系统处于恒定的绝对压力时,当时气体的体积直接变化到其温度。
在数学上

语句2
在恒压下,0℃时每温度变化1℃,所有的理想气体体积变化1/273。
让
什么是绝对零度温度?
因为在0°C时,温度每下降1°C,气体的体积就减少了原始体积的1/273。如果温度是-273°C,那么气体的体积减小到0。
调用气体体积等于零的温度绝对零度的温度。
Gay-Lussac的法律
这项法律于1809年由约瑟夫路易斯同性恋者提供。
声明
在体积不变的情况下,给定质量的理想气体的绝对压强随其绝对温度的变化而变化。
在数学上

其中后缀1、2和3…表示不同的条件集。
解释:

让我们采取一种活塞式气缸组件,其具有理想的气体。活塞不可移动。由于活塞固定,因此体积是恒定的。现在向气缸中存在的气体增加一些热量。气体的温度开始增加并增加气体的压力。可以在附着在系统上的压力表上看到压力的增加。
上述实验证明,在体积不变的情况下,理想气体的压力与其温度成正比。
4.阿伏伽德罗定律
阿伏伽德罗定律有时也被称为阿伏伽德罗假说或阿伏伽德罗原理。它是由阿梅代奥·阿伏伽德罗在1811年提出的一条实验性法则。
声明:
在恒定的温度和压强下,等体积的所有气体包含相等的分子。
或
对于给定质量的理想气体,鉴于温度和压力是恒定的,气体的体积与气体的物质(摩尔数)的量成正比。
在数学上
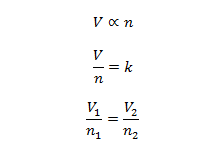
后缀1,2表示一种气体的不同条件集。
在哪里
v =气体的体积。
N =气体的物质量(单位为摩尔)。
k =常数,等于RT/P,其中R是通用气体常数,T是开尔文温度P是压强。因为温度和压强是恒定的,所以RT/P也是恒定的,用k表示。
5.一般气体方程或理想气体定律
理想气体定律或一般气体方程是波依耳定律、查理定律和阿伏伽德罗定律的组合形式。理想气体方程可以写成

在哪里
ρ=气体密度= m / v
p =气体的压力
v =气体的体积
n =气体物质(以摩尔)
r =理想或通用气体常数
T =气体的绝对温度
概述所有三种天然气法律(即博伊尔法律,查尔斯法和Gay-Lussac法)如下所示:

如果你在理解这些气体定律方面有任何困难,你可以通过评论来问我你的问题。如果你觉得这个话题有价值,请分享给别人。